
محققان درحال توسعه آنتیبیوتیکهایی هستند که میتواند از مقاومت وحشتناکی که نسل فعلی آنتیبیوتیکها در میکروبهای بدن ما ایجاد میکنند، فرار کند.
حدود یک دهه پیش، گروهی از محققان به همراه پروفسور «گیلرمو بازان»، استاد شیمی دانشگاه کالیفرنیا سانتا باربارا، شروع به مشاهده یک چالش تکراری در تحقیقات خود کردند: برخی از ترکیباتی که آنها برای مهار انرژی از باکتریها تولید میکردند، درعوض میکروبها را از بین میبرد.
اگر هدف پروژه مهار متابولیسم باکتریهای زنده برای تولید برق باشد، این رویداد خوب نیست.
«الکس مورلند»، عضو فوق دکتری بنیاد سیستیک فیبروزیس که در سال 2014 به گروه تحقیقاتی بازان پیوست گفت: «ما به زندهبودن باکتریها نیاز داشتیم. اما زمانی که درحال توسعه مولکولهای جدید برای آن کاربرد بودیم، متوجه شدیم که برخی از آنها کار نمیکنند زیرا باکتریها را میکشند.»
بااینحال، تیم بهجای اینکه آن را بهعنوان یک مورد آزمایشگاهی نسبتاً آزاردهنده کنار بگذارد، در تحقیقات بعدی به خواص ضدمیکروبی ظاهری این ترکیبات، که الیگوالکترولیتهای مزدوج (COE) نام دارند، جلب شد.
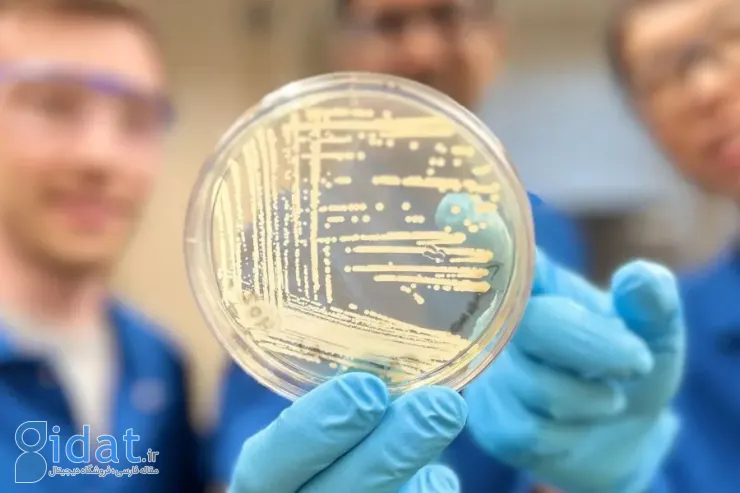
حالا یک فلش فوروارد به امروز میزنیم؛ آنها اکنون پایه و اساس دسته جدیدی از آنتیبیوتیکها را دارند. آنتیبیوتیکی که نهتنها دربرابر طیف وسیعی از عفونتهای باکتریایی نویدبخش است، بلکه میتواند از مقاومت وحشتناکی که نسل فعلی آنتیبیوتیکها در میکروبهای بدن ما ایجاد میکنند، فرار کند.
بازان گفت: «ما متوجه شدیم که چارچوبهای مولکولی که مدتی روی آن کار میکردیم، اگر بهدرستی طراحی شوند، میتوانند دسته جدیدی از آنتیبیوتیکها را تولید کنند؛ چیزی که بهندرت یافت میشود و پیامدهای عمیقی برای پزشکی مدرن دارد.»
مقاومت ضدمیکروبی (AMR) یک مشکل جهانی است که همه جنبههای زندگی را تحت تأثیر قرار میدهد. در سال 2019، حدود 1.3 میلیون مرگ در سراسر جهان را میتوان به AMR نسبت داد.
مورلند میگوید: «این آمار فرض میکند که اگر باکتری مقاوم با یک باکتری غیرمقاوم از همان نوع جایگزین میشد، بیماران زنده میماندند. این مرگومیرهای بیشازحد مربوط به مقاومت به آنتی بیوتیکها هستند و در سالهای گذشته تأثیرگذار بودهاند.»
وی افزود: «در بسیاری از موارد، میزان مرگومیر برای عفونت با برخی از باکتریهای مقاوم، سه برابر بیشتر از سویههای غیرمقاوم است.»
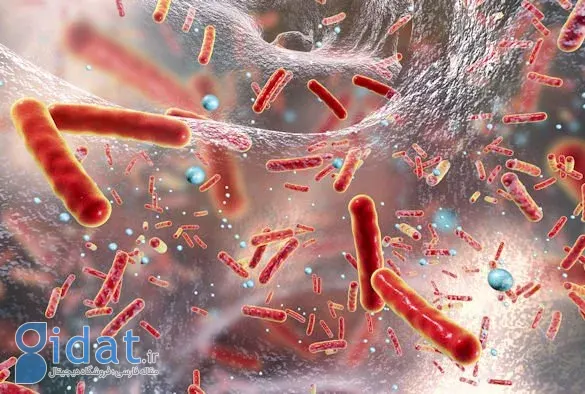
مقاومت آنتیبیوتیکی زمانی ایجاد میشود که باکتری در معرض آنتیبیوتیک قرار میگیرد و راههایی برای شکست یا دورزدن آن ایجاد میکند. استراتژیها شامل استفاده از غشای سلولی بهعنوان یک مانع، ازبینبردن مولکول آزاردهنده یا حذف آن از سلول، یا تغییر هدف دارو برای بیاثرکردن آنتی بیوتیک است. این مکانیسمهای مقاومتی میتوانند به باکتریهای نسل بعدی منتقل شوند یا با سایر باکتریهای محیط به اشتراک گذاشته شوند.
بازان میگوید: «در سال 2019، 4.95 میلیون مرگ مرتبط با مقاومت آنتیبیوتیکی وجود داشت، ازجمله 1.3 میلیون مرگ که میتواند مستقیماً به AMR نسبت داده شود. درحالیکه حدود 10 میلیون نفر هر سال بر اثر سرطان میمیرند. اما آخرینباری که بررسی کردیم، 27 کارآزمایی بالینی برای آنتیبیوتیکهای جدید و 1300 مورد برای درمانهای ضد سرطان انجام شد.»
تیم بینالمللی پژوهشگران نشان میدهند که COEها با بازسازی غشاهای باکتریایی به چندین هدف ضربه میزنند. این تیم به سرپرستی «کایکسی ژانگ»، ترکیبات را علیه یک میکروب مقاوم به نام «مایکوباکتریوم آبسوس» (Mab) به کار بردند که عفونتهای آن دربیماران مبتلا به بیماریهای زمینهای ریوی شایع است.
Mab نهتنها دارای پوشش سلولی غیرعادی ضخیم و غیرقابل نفوذ است که آنتیبیوتیکها را دفع میکند، بلکه این توانایی را دارد که در داخل فاگوسیتها، سلولهای ایمنی که وظیفه آنها بلعیدن و کشتن میکروارگانیسمها است، پنهان شود.
اما نتیجه در مقابل Mab این بود که ترکیبات بهطور مؤثر، باکتریهای آن را از بین نمیبرند و حتی ممکن است ناخواسته آنها را دربرابر آنتیبیوتیکها پنهان کنند.
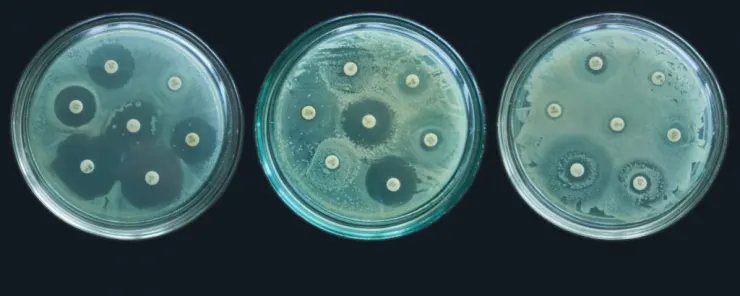
درمانهای فعلی اغلب با وجود دورههای طولانی با سه تا چهار ترکیب از آنتیبیوتیک به مدت 12 تا 18 ماه، شکست میخورد. بیش از نیمی از بیماران درمان نمیشوند و بیش از 70 درصد آنها نیز از عوارض جانبی قابلتوجهی رنج میبرند.
COE در این مطالعه نسبت به آنتیبیوتیکهای آمیکاسین و ایمیپنم در ریشهکنی Mab مؤثرتر بود. محققان این اثربخشی را به هدف قرار دادن این ترکیب بر یکپارچگی فیزیکی و عملکردی دیواره سلولی باکتری نسبت میدهند. این حمله اختلال تأثیری چندبرابری روی باکتریها دارد و ایجاد مقاومت را برای آنها در مقایسه با آنتیبیوتیکهای معمولی 10 تا 1000 برابر دشوارتر میکند.
مکانیسم منحصربهفرد COEها در جنبه دیگری از مقاومت یا تحمل آنتیبیوتیک نیز نقش بسزایی دارد: تولید یک بیوفیلم. بیوفیلم حالتی است که در آن جامعهای از میکروبها بههم متصل میشوند و یک ماده پلیمری تولید میکنند که مانند نوعی سپر است.
آزمایشگاه بازان همچنین COEهایی را توسعه داده است که برای باکتریها بسیار انتخابی است. مورلند و تیمش در «ارتباطات شیمیایی» بررسی کردند که چگونه میتوانند فعالیت آنتیبیوتیکی آنها را بدون اثرات «شبه شوینده» افزایش دهند. در مواد شوینده، اثر ضد باکتریایی به تخریب بیرویه غشای سلولی بستگی دارد.
او گفت: «سلولهای پوست شما در تحمل صابونها و مواد شوینده بسیار خوب هستند، اما سلولهای دیگر بدن، بهویژه گلبولهای قرمز خون، بسیار حساس هستند.»
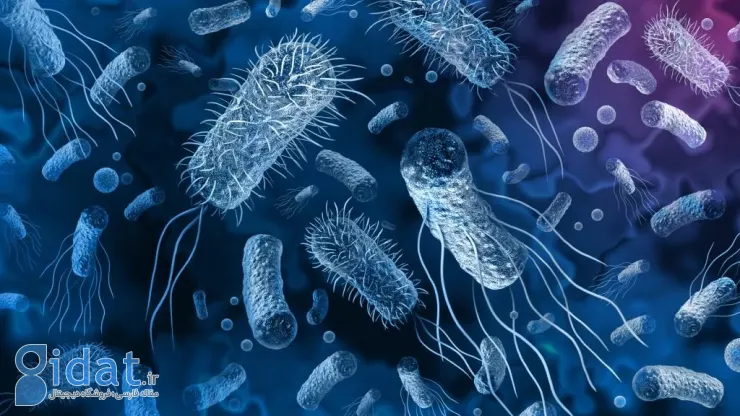
عوامل آنها دریافتند برای COEها، نفوذپذیری غشاء و عملکرد آنتی بیوتیکی ذاتاً به هم مرتبط نیستند. این مکانیسمی است که میتواند برای غشای باکتری نسبت به غشای پستانداران بسیار انتخابی باشد. برای مثال، مولکولهای آزمایش Mab توانستند به داخل فاگوسیتها برسند تا باکتریها را بدون آسیبرساندن به سلولهای پستانداران از بین ببرند.
مورلند گفت: «ما هنوز مکانیسمهای دقیق را نمیدانیم، اما میتوانیم بهطور قطع نشان دهیم که COE باکتریها را میکشد ولی سلولهای پستانداران را نمیکشد. این موضوع لزوماً درمورد مولکولهای اصلی که ما در اوایل کشف کردیم، صدق نمیکرد، اما با کمک ابزارهایی مانند یادگیری ماشینی و شیمی، توانستیم تعیین کنیم که کدام ساختار مولکولی این تعادل را بین اثربخشی دربرابر باکتریها و ایمنی برای پستانداران ایجاد میکند.»
هنوز روزهای اولیه برای گروه تحقیقاتی بازان است، زیرا آنها به بررسی مکانیسمهای عمل، جستجوی خواص جدید و طراحی و اصلاح مولکولهای خود ادامه میدهند. در حالت ایدهآل، آنتیبیوتیکهای COE روزی بهعنوان درمانهای ایمن و مؤثر عمل میکنند که حتی در برابر مقاومترین عفونتهای باکتریایی نیز مؤثر هستند.

بااینحال، مسیر آزمایشهای بالینی طولانی است. مورلند گفت: «تا اینجا همهچیز خیلی خوب است. COEها در آزمایشهایی که انجام دادهایم به خوبی کار کردهاند.»
وی افزود که مولکولهای موجود در این مطالعات، قبل از پیشرفت در آزمایشهای بالینی نیاز به پالایش بیشتری دارند. بدیهی است که توسعه بیشتری موردنیاز است و محققان درحال انجام آن هستند.
پاسخ ها