دانشمندان ویروسهای غولپیکری را کشف کردهاند که دارای ویژگیهایی هستند که پیش از این تنها در سلولهای زنده دیده شده بود.
پژوهشگران با بررسی ژنهای موجود در محیطهای مختلفی مانند بزاق انسان، مدفوع حیوانات، بیمارستانها، خاک و موارد دیگر، صدها ویروس غولپیکر پیدا کردهاند. برخی از این ویروسها دارای قابلیتهایی هستند که تا پیش از این تنها در حیات سلولی دیده شده بود.
یک گروه پژوهشی بینالمللی تحت هدایت دانشمندانی از دانشگاه برکلی کالیفرنیا گروههای کاملا جدیدی از فاژهای غولپیکر را پیدا کردهاند (ویروسهایی که باکتریها را آلوده میکنند) و ۳۵۱ توالی ژنی را با هم ترکیب کردند. پژوهشگران درون این توالیها، ژنهایی را پیدا کردند که ویژگیهای غیرمنتظرهای را کدگذاری میکردند ازجمله بخشهایی از دستگاه سلولی را که دستورالعملهای DNA را برای ساخت پروتئین خوانده و اجرا میکند (فرایند ترجمه). باسم الشايب و جیل بانفیلد از دانشگاه برکلی در مصاحبه با ساینسآلرت گفتند:
آنها دارای تعداد غیرمعمولی از اجزای دستگاه ترجمه هستند که در یک ویروس معمولی دیده نمیشود.
فرایند ترجمه در ساختارهای مولکولی موسوم به ریبوزمها صورت میگیرد و پژوهشگران واقعا ژنهایی را پیدا کردند که برخی از مولفههای آنها (پروتئینهای ریبوزومی) را کدگذاری میکردند. روهان ساچدوا متخصص اکولوژی میکروبی از دانشگاه برکلی گفت:
بهطور معمول، چیزی که زنده را از غیرزنده جدا میکند، داشتن ریبوزوم و توانایی ترجمه است. این یکی از مهمترین ویژگیهایی است که ویروسها را از باکتریها جدا میکند. برخی از فاژهای بزرگ دارای ماشینآلات ترجمه زیادی هستند، بنابراین این مرزبندی را تا حدودی مبهم میکنند.
پژوهشگران همچنین توالیهای کدکنندهی سیستم کریسپر را نیز پیدا کردند. سیستم کریسپر بهعنوان سیستم ایمنی که باکتریها از آن برای مقابلهبا ویروسها استفاده میکنند، نیز وجود دارد. ویروسهای تازه کشفشده همه دارای ژنومهایی با طول بیش از ۲۰۰ هزار جفت نوکلئوتید هستند درحالیکه میانگین اندازهی ژنوم فاژهای شناختهشده، بیشتر و درحدود ۵۲ هزار جفت باز است.
برخی از ژنومهای فاژی که پژوهشگران شناسایی کردند واقعا غولآسا بودند؛ پژوهشگران یک گروه را «فاژهای غولآسا» نامیدند و در نامگذاری ۹ گروه جدید دیگر نیز از کلمهی «بزرگ» استفاده کردند. الشايب و بانفیلد گفتند:
ژنوم این فاژها حداقل ۴ برابر ژنوم یک فاژ معمولی است و بزرگترین آنها ۱۵ برابر حالت معمول بوده و ۷۳۵ هزار جفت باز دارد.
تصور میشود این فاژهای بزرگتر باعث آلودهشدن باکتروئیدها شوند. باکتروئیدها گروهی از باکتریها هستند که بهطور گسترده در محیط پیراموان ما و از خاک گرفته تا رودههای ما حضور دارند. ژنوم این فاژهای سنگین به اندازهی کافی بزرگ است که رقیب ژنوم باکتریهای کوچک شود اما پاندورا ویروسهای آلودهکنندهی آمیب همچنان با ۲/۵ میلیون جفت باز، مقام اول بزرگترین ژنوم ویروسی را دارند. ساچدوا گفت:
فاژهای بزرگی قبلا شناسایی شدهاند اما آنها یافتههای پراکندهای بودند. چیزی که ما در این مقاله پیدا کردیم، آن است که اینها اساسا همه جا هستند. ما آنها را درجایی میبینیم.
همچون سایر فاژها، این گروهاز ویروسها، DNA خود را به میزبان باکتریایی خود تزریق میکنند و تجهیزات تکثیر ژن قربانی را برای ساخت نسخههای از خودشان به خدمت میگیرند. پژوهشگران گمان میکنند که حین این اتفاق، فاژهای غولپیکر همچنین از برخی از ژنهای اضافی خود برای تغییر مسیر مراحل اولیه ترجمه درون باکتری استفاده میکنند و تولید پروتئین را متناسب با نیاز خود منحرف میکنند. چنین کنترلی از تولید پروتئین در ویروسهای جانوری دیده شده است.
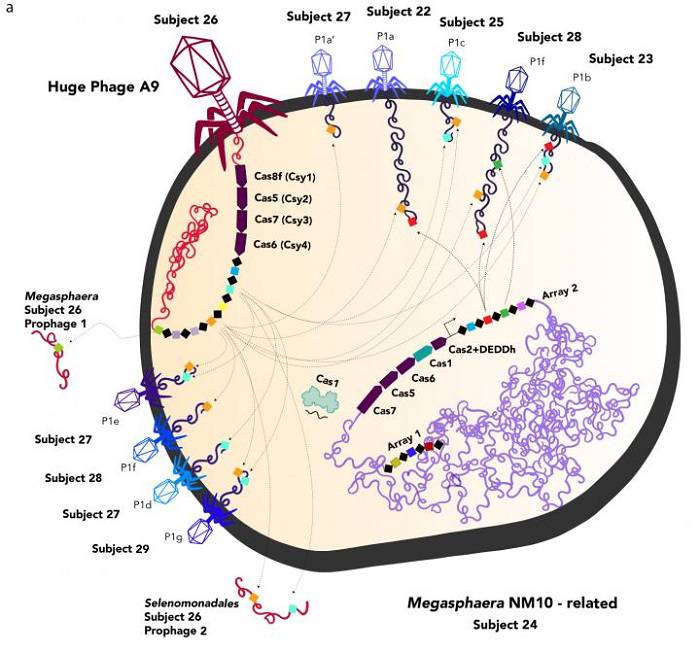
یک فاژ غولپیکر (مورد ۲۶) یک باکتری را آلوده کرده و پاسخ آن دربرابر فاژهای دیگر را دستکاری میکند
الشايب توضیح داد که فاژهای غولپیکر از سیستم کریسپر خود برای جنگ فاژ دربرابر فاژ استفاده میکنند و ویروسهای رقیبی را که قصد دارند همان باکتری میزبان را آلوده کنند، بهطور اختصاصی مورد هدف قرار میدهند. مطالعهای که در سال گذشته منتشر شد، نشان داد که چگونه برخی از فاژها از این سیستم برای خنثیکردن اقدامات ضدفاژی باکتری میزبان استفاده میکنند. بانفیلد گفت:
چیزی که با نگاه کردن به این ژنومهای بزرگ متوجه میشویم، آن است که فاژها ژنها و مسیرهای مختلف زیادی را بهدست آوردهاند؛ برخی از آنها را میتوانیم پیشبینی کنیم و برخی را نیز نمیتوانیم پیشبینی کنیم زیرا درجریان عفونت، فاژ واقعا کنترل عملکرد میزبان باکتریایی خود را به دست میگیرد.
هرچه درمورد ارتباطات بین سلامت جسم و روان و میکروبهایی که درون بدن و محیط پیرامون زندگی میکنند، دانش بیشتری کسب میکنیم، بیشتر متوجه میشویم که هرچیزی که روی این جوامع باکتریایی اثر بگذارد، میتواند تاثیر عمیقی روی ما نیز داشته باشد. الشایب گفت:
فاژها همچنین به انتقال ژنهای کدکنندهی سموم باکتریایی و مقاومت آنتیبیوتیکی بین باکتریها معروف هستند. از آن جایی که ما هم باکتریهای مفید و هم باکتریهای مضر را داریم که روی سطح بدن و نیز داخل بدن ما زندگی میکنند، درک اینکه چه انواعی از فاژها همراه باکتریها در بدن انسانها و حیوانات وجود دارند و چگونه روی محیطهای مذکور تاثیر میگذارند، از اهمیت زیادی برخوردار است.
پژوهشگران پیشنهاد میکنند که سیستمهای کریسپری که برخی از این فاژها دارند، شاید این قابلیت را داشته باشد که به ما کمک کند تا با تغییر عملکرد باکتریها یا حذف باکتریهای مشکلساز، میکروبیوم خود را کنترل کنیم. الشايب و بانفیلد اکنون امیدوارند که برخی از این فاژهای غولآسا را در آزمایشگاه پرورش دهند تا درمورد سیستمهای کریسپر فاژها دانش بیشتری بهدست آورند و نقشهای آنها را کشف کرده و ارزش آنها را در ویرایش ژن ارزیابی کنند. کریستوف ویگل، متخصص بیوشیمی که در این مطالعه مشارکتی نداشته است، میگوید مقالهی حاضر از ایدهی درنظرگرفتن ویروسها بهعنوان «ویروسل زنده» حمایت میکند. بانفیلد توضیح داد:
این فاژهای عظیم، شکاف بین «باکتریوفاژهای غیرزنده» و «باکتریها و آرکیاها» را پر میکنند. قطعا استراتژیهای موفقی برای زندگی وجود دارد که ترکیبی از ویروس معمولی و ارگانیسمهای زنده معمولی است.
اگرچه مطالعهی حاضر درمورد تنوع زیستی ویروسها نیز دانش زیادی همراه خود دارد، درحالحاضر، مهمترین بحثی که پیش میآید، معنای واقعی زنده بودن است.
نتایج این پژوهش در مجلهی Nature منتشر شده است.
پاسخ ها